Proteinuria: Il rene parla attraverso le urine
La proteinuria non è un semplice dato laboratoristico: è un segnale diretto di sofferenza renale e un marker indipendente di rischio cardiovascolare e di mortalità nella popolazione generale.
30 Aprile 2026
Scritto da: Ing. Brattoli Luca, Marketing scientific manager
Introduzione
La proteinuria non è un semplice dato laboratoristico: è un segnale diretto di sofferenza renale e un marker indipendente di rischio cardiovascolare e di mortalità nella popolazione generale.
Il rene, attraverso la perdita di proteine nelle urine, comunica un’alterazione del proprio sistema di filtrazione glomerulare e/o di riassorbimento tubulare. Spesso lo fa in silenzio, senza sintomi evidenti, rendendo fondamentale il ruolo del laboratorio nell’identificazione precoce.
Intercettare la proteinuria significa intervenire prima che il danno diventi irreversibile — in un’ottica preventiva, prognostica e terapeutica.
Proteinuria: un marker chiave di danno renale
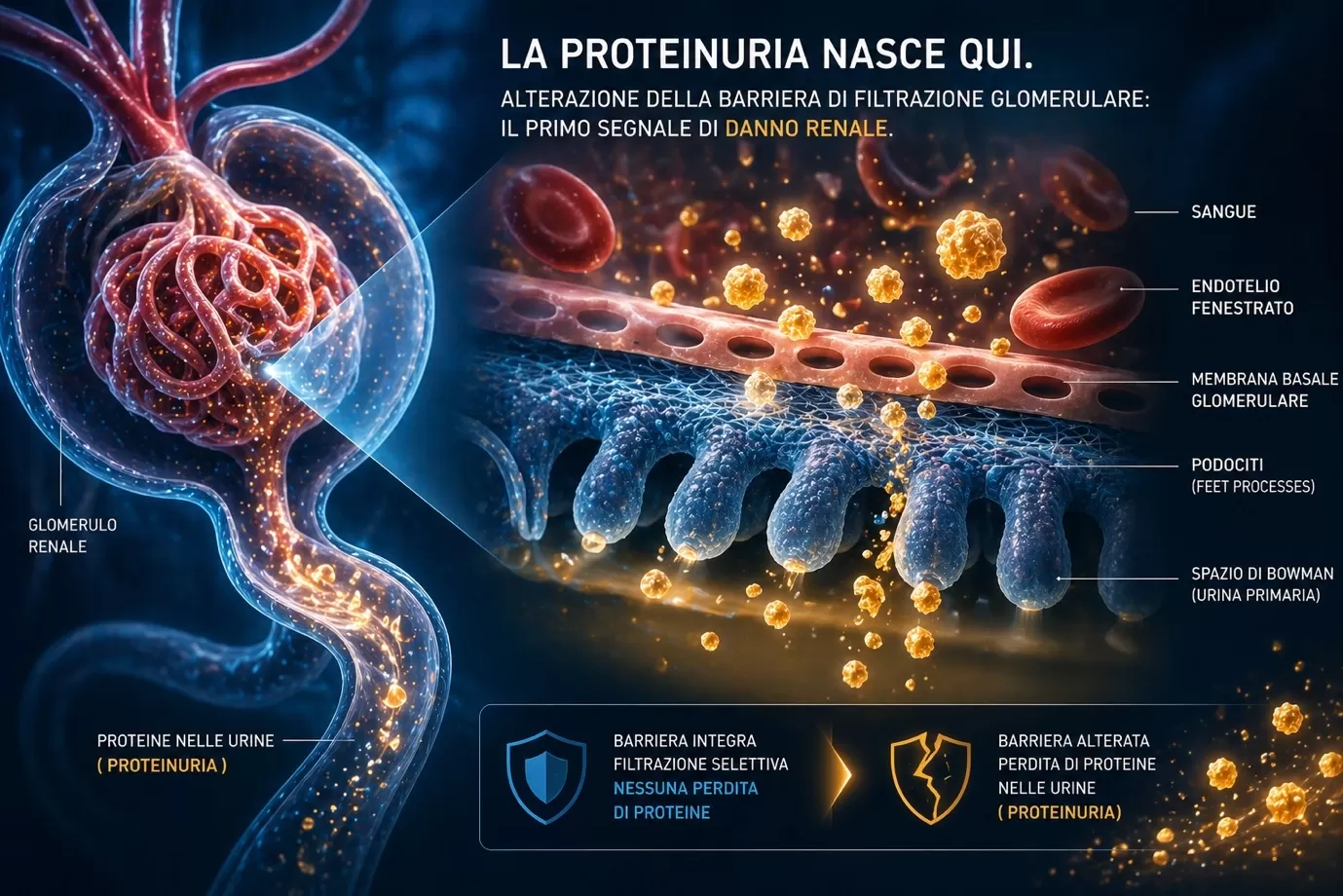
In condizioni fisiologiche, la barriera di filtrazione glomerulare — costituita da endotelio fenestrato, membrana basale glomerulare e podociti — impedisce il passaggio nelle urine delle proteine plasmatiche di peso molecolare elevato. Una quota minima di proteine a basso peso molecolare attraversa il filtro e viene riassorbita dal tubulo prossimale. L’escrezione totale fisiologica è inferiore a 150 mg/24h.
Quando la barriera glomerulare o il riassorbimento tubulare sono compromessi, anche in modo lieve, si manifesta proteinuria.
Le principali condizioni associate includono:
- Nefropatie glomerulari primitive e secondarie
- Diabete mellito (nefropatia diabetica)
- Ipertensione arteriosa (nefroangiosclerosi)
- Malattie sistemiche (LES, vasculiti, amiloidosi, mieloma multiplo)
- Malattia renale cronica (CKD)
Secondo la classificazione KDIGO, l’albuminuria viene stratificata in tre categorie prognostiche basate sul rapporto albumina/creatinina urinaria (UACR):
- A1 — normale o lievemente aumentata: < 30 mg/g (< 3 mg/mmol)
- A2 — moderatamente aumentata: 30–300 mg/g (3–30 mg/mmol)
- A3 — severamente aumentata: > 300 mg/g (> 30 mg/mmol)
Dal punto di vista clinico, la proteinuria rappresenta:
- un indicatore precoce di danno renale
- un fattore prognostico indipendente di progressione verso l’insufficienza renale terminale
- un predittore robusto di eventi cardiovascolari e mortalità, dimostrato da ampi studi epidemiologici e meta-analisi della popolazione generale
- un parametro fondamentale nel monitoraggio della progressione di malattia e della risposta terapeutica
Non si tratta quindi solo di rilevare la presenza di proteine, ma di quantificarle con precisione e seguirne l’evoluzione nel tempo.
Albuminuria moderatamente aumentata: la fase precoce
All’interno dello spettro della proteinuria, ciò che storicamente è stato definito microalbuminuria — oggi più correttamente denominato albuminuria moderatamente aumentata o categoria A2 secondo KDIGO — rappresenta la fase iniziale del danno renale, caratterizzata da una modesta ma non fisiologica escrezione di albumina (UACR 30–300 mg/g).
È particolarmente rilevante nei pazienti diabetici e ipertesi, in cui costituisce un marker predittivo precoce di nefropatia, ed è stata associata a un aumento significativo del rischio cardiovascolare già a partire da valori al limite superiore della norma.
Il suo significato clinico va letto come un continuum di danno:
☞ albuminuria moderata (A2) → albuminuria severa (A3) → CKD avanzata
Per questo motivo, la vera sfida non è solo identificare la fase precoce, ma non perdere il momento in cui evolve in proteinuria clinicamente significativa. Studi longitudinali hanno dimostrato che una riduzione dell’albuminuria nel tempo si associa a una riduzione del rischio di progressione verso l’end-stage renal disease (ESRD), confermando il valore della quantificazione seriata e standardizzata.
Limiti dello screening tradizionale
Le strisce reattive (dipstick) rappresentano ancora oggi il primo livello di screening dell’esame chimico delle urine, ma presentano limiti documentati:
- Sensibilità limitata alle basse concentrazioni di albumina (cut-off semiquantitativo tipicamente intorno a 150–300 mg/L)
- Falsi negativi in urine diluite (densità < 1.005) o con escrezione di proteine non rilevate dal reattivo (catene leggere, microglobuline)
- Falsi positivi in urine alcaline (pH > 8), in presenza di clorexidina, mezzi di contrasto iodati, ematuria macroscopica o emoglobinuria
- Variabilità interpretativa legata all’operatore nelle letture visive
- Mancata stratificazione della categoria A2 (albuminuria moderatamente aumentata), proprio quella diagnosticamente più rilevante
Le linee guida KDIGO e le raccomandazioni intersocietarie italiane (SIBioC–SIPMeL–SIN, Gruppo GIAU) e dell’European Confederation of Laboratory Medicine indicano l’UACR su campione spot come metodo di riferimento per lo screening e il monitoraggio dell’albuminuria, in alternativa alla raccolta delle 24 ore.
L’analisi automatizzata, integrata in un workflow strutturato, supera molti di questi limiti e garantisce:
- standardizzazione del processo
- maggiore sensibilità analitica
- riduzione della variabilità operatore-dipendente
- piena tracciabilità dei risultati
RT-U600 di REETOO: l’evoluzione dell’analisi urinaria

Nel contesto della diagnostica moderna, RT-U600 di REETOO rappresenta una soluzione concreta per migliorare l’accuratezza e l’efficienza dell’analisi urinaria.
Il sistema consente:
- Rilevazione sensibile e standardizzata della proteinuria
- Analisi automatizzata con riduzione dell’errore umano
- Elevata riproducibilità dei risultati
- Workflow rapido, adatto anche ad alti volumi di campioni
- Integrazione nei sistemi laboratoristici digitali e nel LIS
A differenza dello screening manuale, RT-U600 permette una valutazione più affidabile e oggettiva, fondamentale quando si tratta di identificare variazioni anche minime ma clinicamente rilevanti.
In particolare, nella gestione della proteinuria:
- migliora la capacità di screening precoce della popolazione a rischio
- supporta il monitoraggio nel tempo dei pazienti con CKD, diabete e ipertensione
- riduce il rischio di falsi negativi nelle fasi iniziali
- contribuisce a una refertazione strutturata e tempestiva
Dalla rilevazione alla gestione clinica
Una proteinuria identificata precocemente cambia il percorso del paziente.
Permette di:
- rallentare la progressione del danno renale (terapia con RAAS-inibitori, SGLT2-inibitori, controllo pressorio)
- ottimizzare il controllo metabolico nel paziente diabetico
- ridurre il rischio cardiovascolare, strettamente correlato all’albuminuria anche nei range storicamente considerati “non patologici”
- personalizzare il follow-up in funzione della categoria di rischio KDIGO (matrice eGFR × albuminuria)
- In questo processo, il laboratorio non è solo esecutore, ma parte attiva nella decisione clinica.
Strumenti come RT-U600 rendono questo ruolo ancora più centrale, restituendo al clinico un dato sensibile, standardizzato e tempestivo.
L'importanza della valutazione morfologica: il caso della proteinuria "falsa"
Un aspetto critico, spesso sottovalutato dai sistemi di automazione chimica, è la possibile interferenza causata dalla presenza di spermatozoi nel campione urinario. Questi elementi cellulari, se presenti in quantità significativa, possono causare un aumento aspecifico della proteinuria totale. Mentre lo strumento rileva correttamente la presenza di proteine nel campione, non è in grado di distinguere se tale valore sia dovuto a un danno della barriera di filtrazione glomerulare o a una contaminazione da liquido seminale. In questo contesto, l'occhio esperto del biologo attraverso l'analisi del sedimento urinario è l'unico strumento capace di identificare la reale causa del dato alterato, evitando al paziente inutili allarmismi o approfondimenti diagnostici per una sospetta nefropatia che, in realtà, è un falso positivo clinico.
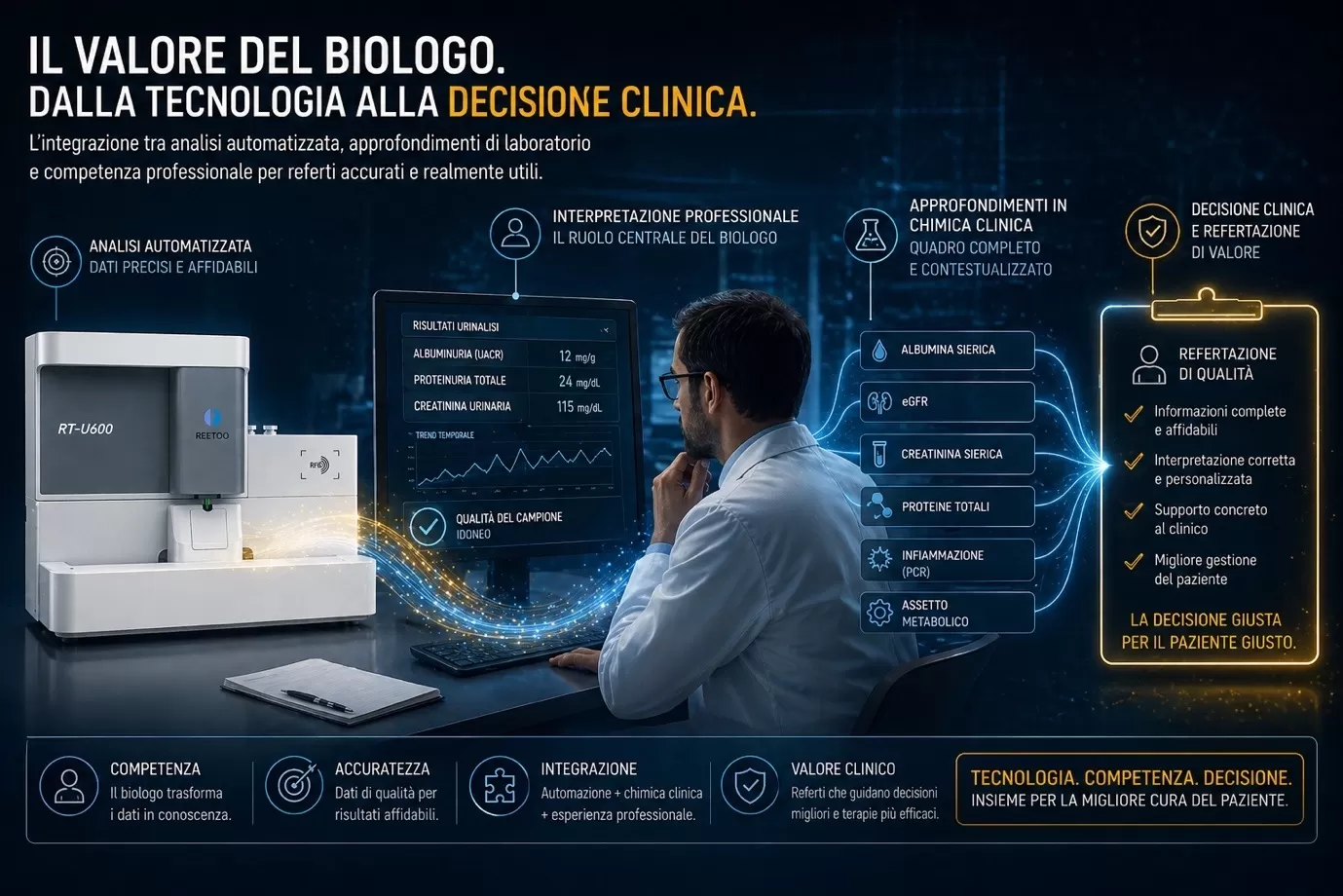
Il Valore del Biologo: Dalla Tecnologia alla Decisione Clinica
In questo scenario di avanzamento tecnologico, il ruolo del biologo di laboratorio emerge come il vero ponte tra il dato analitico e la gestione del paziente. Se da un lato sistemi come RT-U600 garantiscono l'accuratezza e la standardizzazione necessarie a rilevare anche minime variazioni di albuminuria (categoria A2), dall'altro è la competenza professionale a trasformare quel numero in una decisione clinica di valore. Il biologo non si limita a validare un risultato, ma ne garantisce l'appropriatezza clinica integrando i parametri urinari con il quadro biochimico complessivo (eGFR, creatinina sierica, assetto metabolico) e assicurando la qualità del campione. Questa sinergia tra automazione di precisione e interpretazione specialistica permette di fornire al clinico referti realmente predittivi, assicurando che ogni paziente riceva la diagnosi corretta nel momento più opportuno per cambiare la storia naturale della malattia.Conclusioni
La proteinuria è uno dei segnali più importanti che il rene può inviare. Ignorarla significa perdere tempo prezioso, sia in termini di prognosi renale sia di rischio cardiovascolare globale.
Oggi, grazie a tecnologie avanzate come RT-U600 di REETOO, è possibile intercettare questo segnale in modo più preciso, rapido e affidabile, in linea con quanto raccomandato dalle linee guida internazionali e nazionali.
Non si tratta più solo di fare un esame delle urine.
Si tratta di trasformarlo in uno strumento diagnostico strategico.
Perché quando il rene parla, serve la tecnologia giusta per ascoltarlo davvero.
Bibliografia
Stevens PE, Ahmed SB, Carrero JJ, Foster B, Francis A, Hall RK, et al. KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int. 2024;105(4S):S117–S314.
Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int Suppl. 2013;3(1):1–150.
Mogensen CE. Microalbuminuria predicts clinical proteinuria and early mortality in maturity-onset diabetes. N Engl J Med. 1984;310(6):356–360.
Hillege HL, Fidler V, Diercks GFH, van Gilst WH, de Zeeuw D, van Veldhuisen DJ, et al. Urinary albumin excretion predicts cardiovascular and noncardiovascular mortality in general population. Circulation. 2002;106(14):1777–1782.
Gerstein HC, Mann JFE, Yi Q, Zinman B, Dinneen SF, Hoogwerf B, et al. Albuminuria and risk of cardiovascular events, death, and heart failure in diabetic and nondiabetic individuals. JAMA. 2001;286(4):421–426.
Matsushita K, van der Velde M, Astor BC, Woodward M, Levey AS, de Jong PE, et al. Association of estimated glomerular filtration rate and albuminuria with all-cause and cardiovascular mortality in general population cohorts: a collaborative meta-analysis. Lancet. 2010;375(9731):2073–2081.
Coresh J, Heerspink HJL, Sang Y, Matsushita K, Arnlov J, Astor BC, et al. Change in albuminuria and subsequent risk of end-stage kidney disease: an individual participant-level consortium meta-analysis. Lancet Diabetes Endocrinol. 2019;7(2):115–127.
Levey AS, de Jong PE, Coresh J, El Nahas M, Astor BC, Matsushita K, et al. The definition, classification, and prognosis of chronic kidney disease: a KDIGO Controversies Conference report. Kidney Int. 2011;80(1):17–28.
Kouri T, Fogazzi G, Gant V, Hallander H, Hofmann W, Guder WG. European urinalysis guidelines. Scand J Clin Lab Invest Suppl. 2000;231:1–86.
White SL, Yu R, Craig JC, Polkinghorne KR, Atkins RC, Chadban SJ. Diagnostic accuracy of urine dipsticks for detection of albuminuria in the general community. Am J Kidney Dis. 2011;58(1):19–28.
Manoni F, Gessoni G, Fogazzi GB, Alessio MG, Caleffi A, Gambaro G, et al. Esame fisico, chimico e morfologico delle urine: proposta di linee guida per la fase analitica del Gruppo Intersocietario Analisi delle Urine (GIAU). Biochim Clin. 2016;40(4):353–383.